1.1. Закон осмотического давления Вант — Гоффа (1887 г.)
Осмос – это односторонняя самопроизвольная диффузия молекул растворителя через полупроницаемую мембрану из раствора с низкой концентрацией в раствор с высокой концентрацией.
Осмотическим давлением (π) называется гидростатическое давление, которое надо приложить к раствору, чтобы задержать осмос.
Осмотическое давление не зависит от природы растворителя и растворенного вещества. При постоянной температуре оно определяется числом « кинетических элементов» — молекул, ионов, ассоциатов, коллоидных мицелл в единице объема, то есть является коллигативным свойством.
Осмотическое давление разбавленного раствора равно тому газовому давлению, которое производило бы растворенное вещество, если бы оно в виде газа при той же температуре занимало тот же объем, что и раствор:
π V = nRT (1.1) или
π = с RT (1а), где с = n/V – молярная концентрация растворенного вещества.
Первый закон Рауля (1887 г.)
Давление насыщенного пара над раствором равно его давлению над чистым растворителем, умноженному на молярную долю растворителя:
Р = ро χо (1.2),
Где ро – давление паров над чистым растворителем, р – давление паров над раствором, χо – молярная доля растворителя.
Несложные преобразования уравнения (1.2) позволяют получить другую зависимость:
χ = ро – р / ро (1.3),
Где χ = n/n + no – молярная доля растворенного вещества.
При постоянной температуре относительное понижение давления насыщенного пара над раствором нелетучего вещества равно молярной доле этого вещества в растворе.
Для разбавленных растворов (n<<no) выражение (1.3) упрощается:
(ро – р) / ро = n/nо или Δp = po×n/no (1.4).
Δp зависит только от числа частиц в растворе, следовательно, является коллигативным свойством. Так как n = m/M, появляется возможность рассчитать молярную массу растворенного вещества по величине экспериментально найденного понижения давления паров над раствором:
М = Мо×m/mo×po/(po – p) (1.5)
/В формулах (2) – (5) индекс «о» относится к чистому растворителю, а параметр без индекса относится к растворенному веществу/
1.3. Второй закон Рауля (1887 г.):
Понижение температуры замерзания или повышение температуры кипения раствора неэлектролита прямо пропорциональны его моляльной концентрации:
ΔТ = К сm (1.6),
Где сm = m×1000/ M×mо– моляльная концентрация растворенного вещества. Из уравнения (1.6) следует, что растворы с одинаковой моляльной концентрацией вызывают одинаковое изменение температуры замерзания или кипения в одном и том же растворителе, то есть обладают коллигативными свойствами.
При замерзании растворов К – криоскопическая константа растворителя, которая может быть рассчитана по формуле:
Ккр. = RT2/1000 Δh (1.7),
Где Δh – удельная теплота плавления, Дж/г (Для воды в форме льда Δh = 333,3 Дж/г).
При кипении растворов К – Эбулиоскопическая константа растворителя, которая может быть рассчитана по формуле:
Кэб. = RT2/1000 Δl (1.8),
Где Δl – удельная теплота испарения, Дж/г.
/Криоскопическая и эбулиоскопическая константы различных растворителей даны в приложении табл.4.2/
Методы косвенного определения осмотического давления
1) По связи закона Вант — Гоффа со вторым законом Рауля
В разбавленных растворах без существенной погрешности можно принять, что с = сm, тогда сопоставление уравнений (1а) и (6) дает выражение:
π = ΔТ/Ккр.×RT (1.9).
Если в качестве растворителя взята вода, то
π = ΔТ×8,314×273,15/1,86 = 1,22ΔТ (МПа)
2) По связи закона Вант — Гоффа с первым законом Рауля
Сопоставление уравнений (1а) и (2) с учетом изменения химических потенциалов при испарении /Вывод опускается/ ведет к выражению:
V¯× π = RT ln po/p (1.10),
Где V¯= М/ρ — парциальный молярный объем растворителя.
По количественной аналогии между осмотическим и газовым давлением
Если в 22,4 л раствора содержится 1 моль неэлектролита, то осмотическое давление такого раствора при ОоС должно быть равно 101,325 кПа.
Отклонения от законов Вант — Гоффа и Рауля
Рассчитанное по закону Вант — Гоффа осмотическое давление может не совпадать с полученным опытным путем в случаях, когда реальное число химических частиц в растворе будет больше или меньше расчетного. Это может произойти в том случае, если в растворе будут происходить процессы ассоциации или диссоциации молекул растворенного вещества. Оценить глубину отклонения можно с помощью изотонического коэффициента Вант — Гоффа: i = πоп./πтеор. При значениях коэффициента больше единицы в растворе идет процесс диссоциации, при значениях коэффициента меньше единицы, наоборот, происходит ассоциация.
![]() 1.6. Обучающие задания
1.6. Обучающие задания
1. Определите осмотическое давление децимолярного раствора неэлектролита при ОоС двумя способами.
Решение: Способ 1. 1л раствора содержит 0,1 моль вещества
22,4 л — х = 2,24 моль
При содержании 1 моль вещества в 22,4 л раствора π = 101,325 кПа, тогда при содержании в растворе 2,24 моль вещества π = 2,24×101,325/1 = 227 кПа
Способ 2. Воспользуемся уравнением (1а):
π = 0,1×8,314×273 = 227 кПа
![]() 2. Рассчитайте осмотическое давление одномолярного раствора сахарозы в воде, зная, что при 30оС давление паров над раствором р = 31,207 мм рт. ст., давление паров над водой ро= 31,824 мм рт. ст., а плотность воды ρ30оС = 0,99564 г/см3.
2. Рассчитайте осмотическое давление одномолярного раствора сахарозы в воде, зная, что при 30оС давление паров над раствором р = 31,207 мм рт. ст., давление паров над водой ро= 31,824 мм рт. ст., а плотность воды ρ30оС = 0,99564 г/см3.
Решение: Молярный объем воды при температуре опыта:
V¯= 18,02/0,99564 = 18,10 см3/моль или 0,01810 л/ моль
При выражении объема в литрах, а давления в атмосферах, R = 0,08205. Bоспользовавшись уравнением (10), получим:
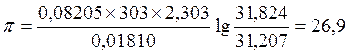 Атм
Атм
Приближенный расчет по формуле (1) дает:
![]()
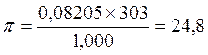 Атм
Атм
3. Упругость пара раствора, содержащего 11,94 г гликокола (С2Н5NН2) в 100 г воды, равна 740,9 мм рт. ст. при 100оС. Какова молярная масса растворенного вещества?
Решение: Воспользуемся формулой (5):
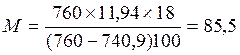 Г/моль
Г/моль
![]() 4. Раствор, содержащий 8 г нафталина С10Н8 в 100 г диэтилового эфира, кипит при 36,33оС, чистый эфир кипит при 35оС. Найти эбулиоскопическую константу эфира.
4. Раствор, содержащий 8 г нафталина С10Н8 в 100 г диэтилового эфира, кипит при 36,33оС, чистый эфир кипит при 35оС. Найти эбулиоскопическую константу эфира.
Решение: ΔТ = 36,33 – 35 = 1,33 о
Кэб. = 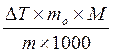 , Кэб.=
, Кэб.=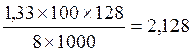
![]() 5. Осмотическое давление разбавленных растворов является аддитивным свойством, поэтому для решения ряда задач к нему применимо «правило креста» или квадрат Пирсона:
5. Осмотическое давление разбавленных растворов является аддитивным свойством, поэтому для решения ряда задач к нему применимо «правило креста» или квадрат Пирсона:
![]()
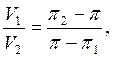 Где
Где ![]()
В каких объемных соотношениях надо смешивать растворы неэлектролитов, имеющих осмотические давления 12 и 3 атм, чтобы получить раствор с давлением 4, 8 атм?
Решение: В соответствии с правилом креста: 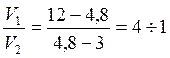
![]()
1.7. Задачи для самостоятельного решения
1. В 1 л раствора содержится 18,4 г глицерина С3Н5(ОН)3 при 17оС. Чему равно осмотическое давление раствора?
2. Осмотическое давление раствора глюкозы при 0оС 454 кПа. Какова молярность раствора?
3. Найти осмотическое давление 5%-ного раствора ацетона (ρ = 0,9 г/мл) при 7оС.
4. В 40 мл раствора содержится 0,72 г неэлектролита. Раствор изотоничен 0,1 М раствору мочевины СО(NН2)2. Найти молярную массу неэлектролита.
5. Антифризы – жидкости с пониженной температурой замерзания, применяемые в системе охлаждения моторов автомобилей и тракторов. Вычислите массу этиленгликоля С2Н4(ОН)2, которую необходимо добавить к
1 кг воды для приготовления антифриза с температурой замерзания -15оС.
6. Температура кипения этилового спирта 78,3оС. Раствор, содержащий 6,57 г йода в 100 г спирта, закипает 78,6оС. Какова молекулярная формула йода?
7. Каково давление пара раствора, содержащего 0,2 моль сахара в 450г воды?
8. Определите молярную массу анилина, зная, что при 30оС давление пара раствора, содержащего 3,09 г анилина в 370 г эфира (С2Н5)2О, равно 643,6 мм рт. ст., а давление пара чистого эфира при той же температуре равно 647,9 мм рт. ст.
9. При растворении 0,94 г фенола в 50 г этилового спирта температура кипения последнего повысилась на 0,232оС. Найти молярную массу фенола.
11. Температура затвердевания чистого бензола 5,5 оС, а раствора
1,632 г трихлоруксусной кислоты СС1СООН в 100 г бензола 5,15 оС. Подвергаются ли молекулы кислоты в бензольном растворе ассоциации или диссоциации и в какой степени?
12. К 10 мл бензола (ρ = 0,879 г/мл) добавили 0,5548 г нафталина. Температура затвердевания полученного раствора 2,981оС. Определите молярную массу нафталина в бензоле, если температура затвердевания чистого бензола 5,5оС, а его теплота плавления Δh =127,4 Дж/г.
13. В 10,6 г раствора салициловой кислоты в этаноле содержится
0,401 г салициловой кислоты. Повышение температуры кипения раствора равно 0,320оС, теплота парообразования этанола Δ1 = 906 Дж/г. Определите молярную массу салициловой кислоты, растворенной в спирте.
14. Сколько воды и раствора неэлектролита (по объему) с осмотическим давлением 20 атм надо взять, чтобы приготовить 5 л раствора с давлением 6 атм.?
15. Температура кипения раствора 12,8 г серы в 250 г бензола на 0,514о выше, чем у чистого растворителя. Выведите молекулярную формулу серы.
16. Из 342 г сахара и воды приготовлено 22,4 л раствора. Найдите осмотическое давление раствора двумя способами.
Физико-химические свойства водных растворов электролитов
2.1. Коллигативные свойства водных растворов электролитов
Электролиты – это вещества, полностью или частично распадающиеся на ионы в растворе или расплаве.
Распад на ионы под действием полярных молекул растворителя называется электролитической диссоциацией.
Сила электролита определяется степенью его диссоциации:
α = Nрасп/Nнач., (2.1)
Где Nнач – число молекул в исходном растворе, Nрасп. – число молекул, распавшихся на ионы. Различают слабые (α < 5%) и сильные электролиты.
Процесс диссоциации слабых электролитов обратим и к нему применим закон действия масс:
КА ↔ К+ + А-
Состояние равновесия характеризуется константой равновесия, которая не зависит от концентрации электролита, а зависит от его природы и температуры:
Кдиссоц.= [K+][A-]/ [KA] (2.2)
Степень диссоциации и константа диссоциации связаны между собой законом разведения Оствальда:
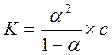 (2.3),
(2.3),
Где с – молярная концентрация, моль/л. Если с <<1 (очень слабые электролиты), то степенью диссоциации в знаменателе можно пренебречь, тогда:
Кдиссоц= α2 с (2.4)
Сильные электролиты диссоциируют в водных растворах практически нацело. Однако активность ионов в значительной степени зависит от концентрации раствора, радиуса гидратированных ионов, заряда ионов. Это приводит к торможению движения ионов в растворе, снижению их активности. Для оценки способности ионов к химическим действиям в растворе вместо концентрации вводится понятие активность.
Активность – эффективная или условная концентрация, соответственно которой электролит ведет себя в химических реакциях:
А = γ с (2.5),
Где γ – коэффициент активности, величина, зависящая от ионной силы раствора. Для электролита, состоящего из однозарядных катиона и аниона, АВ активность можно рассчитать по формуле:
А(АВ) = а+ а — = с2γ +γ — (2.6)
Средняя активность электролита а± = √а+ а — (2.7)
Для электролита с разными зарядами катиона и аниона AmBn:
А± = ![]() (2.8)
(2.8)
Ионная сила раствора (μ) является мерой электростатического взаимодействия между ионами в растворе:
μ = ½ (с1z12 + c2 z22 + … + ci zi2) (2.9),
Где z – заряды ионов, с – концентрация ионов, моль/л.
Коэффициент активности можно рассчитать из ионной силы раствора по уравнению Дебая-Хюккеля:
Lg γ± = 0,5 z2√μ (2.10)
Степень отклонения экспериментальных данных от рассчитанных теоретически учитывает «кажущаяся степень диссоциации»:
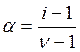 (2.11),
(2.11),
Где ![]() — число ионов, на которые диссоциирует электролит, i – изотонический коэффициент Вант – Гоффа. Он показывает, во сколько раз экспериментально найденные значения коллигативных свойств: осмотического давления, понижения давления паров над раствором, снижения температуры замерзания и повышения температуры кипения раствора электролита превышают ту же величину для раствора неэлектролита той же начальной концентрации:
— число ионов, на которые диссоциирует электролит, i – изотонический коэффициент Вант – Гоффа. Он показывает, во сколько раз экспериментально найденные значения коллигативных свойств: осмотического давления, понижения давления паров над раствором, снижения температуры замерзания и повышения температуры кипения раствора электролита превышают ту же величину для раствора неэлектролита той же начальной концентрации:
I = πэксперим./πвычисл. (2.12)
Сопоставляя значения ν и i, можно оценить меру отклонения раствора электролита от идеального: 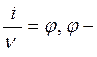 Осмотический коэффициент.
Осмотический коэффициент.
Вывод: Для растворов электролитов в математические выражения законов Вант – Гоффа и Рауля вводится поправочный — изотонический коэффициент i = 1 + α(ν-1):
π V = i nRT (2.12)
Δp = i po n/no (2.13)
ΔТ = i К сm (2.14)
2.1. Обучающие задания
![]() 1. Рассчитайте ионную силу раствора, содержащего 0,01 моль ВаС12 и 0,1 моль NaNO3.
1. Рассчитайте ионную силу раствора, содержащего 0,01 моль ВаС12 и 0,1 моль NaNO3.
Решение: Диссоциация солей в растворе идет по схемам:
NaNO3 = Na+ + NO3-
0,1 0,1 0,1
BaCl2 = Ba2+ + 2Cl-
0,01 0,01 0,02
Воспользовавшись уравнением (2.9), получим:
μ = ½ (0,01× 22 + 0,02× 12 + 0,1× 12 + 0,1× 12) = 0,13
![]() 2. Вычислите активность йодида натрия в растворе, моляльность которого 0,05, если известно, что средний коэффициент активности γ± равен 0,84.
2. Вычислите активность йодида натрия в растворе, моляльность которого 0,05, если известно, что средний коэффициент активности γ± равен 0,84.
Решение: Активность электролита, состоящего из однозарядных ионов, можно рассчитать по формуле (2.6):
A(NaI) = 0,052 × (0,84)2 = 1,76×10-3 моль/кг
![]() 3. Определите кажущуюся степень диссоциации 0,01 М раствора бромида натрия, если изотонический коэффициент равен 1,32.
3. Определите кажущуюся степень диссоциации 0,01 М раствора бромида натрия, если изотонический коэффициент равен 1,32.
Решение: Уравнение диссоциации бромида натрия: NaBr = Na+ + Br-, следовательно, ν = 2. Воспользуемся формулой (2.11):
α =(1,32 -1)/ (2-1) = 0,32 или 32%
![]() 4. Определите атмосферное давление, если 0,1 М раствор поваренной соли кипит при 99,8 оС. Кажущаяся степень диссоциации соли 84,4%. Давление насыщенного пара чистой воды при этой температуре 100600 Па. Плотность раствора равна 1.
4. Определите атмосферное давление, если 0,1 М раствор поваренной соли кипит при 99,8 оС. Кажущаяся степень диссоциации соли 84,4%. Давление насыщенного пара чистой воды при этой температуре 100600 Па. Плотность раствора равна 1.
Решение: При температуре кипения давление пара растворителя над раствором равно атмосферному давлению. Следовательно, использовавши формулу (2.13) и рассчитав давление пара растворителя над раствором, можно определить атмосферное давление.
Найдем изотонический коэффициент: i = 1 + 0,844 = 1,844
В 1 л 0,1 М раствора соли содержится 5,85 г NaCl
Число молей воды no = (1000 – 5,85)/18 = 55,2 моль
Р = Р(атм.) = 100600 – (1,844×0,1×100600)/55,6 = 100264 Па
2.3. Задачи для самостоятельного решения
1. Раствор, содержащий 0,05 моль сульфата алюминия в 100 г воды, замерзает при -4,19 оС. Найти кажущуюся степень диссоциации соли.
2. Определите температуру замерзания водного раствора хлорида кальция, если кажущаяся степень диссоциации соли в растворе примерно равна 1, а концентрация раствора 0,5%.
3. При растворении 19,46 г сульфата натрия в 100 г воды температура кипения повысилась на 1,34 оС. Определите кажущуюся степень диссоциации соли в данном растворе.
4. Осмотическое давление 1 моль бромида калия, растворенного в 8 л воды, равно 5,63×105 Па при 25оС. Определить кажущуюся степень диссоциации соли в данном растворе.
5. Раствор, содержащий 0,4359 моль/л тростникового сахара при 18оС, изотоничен с раствором хлорида натрия, концентрация которого 14,616 г/л. Найти кажущуюся степень диссоциации соли в растворе.
6. Определите температуру кипения 1Н раствора азотной кислоты, если степень диссоциации кислоты в растворе 0,82, а плотность раствора равна плотности чистой воды.
7. Определите степень диссоциации хлоруксусной кислоты в растворе, содержащем 0,945 г кислоты в 100 г воды, если понижение температуры замерзания раствора 0,206о.
8. Определите осмотический коэффициент нитрата калия в водном растворе с моляльной концентрацией 0,1 моль/кг, если понижение температуры замерзания равно 0,336о.
3. Контролирующие задания
3.1. Контрольные вопросы
1. Охарактеризуйте явление осмоса и природу осмотического давления.
2. Сформулируйте закон Вант — Гоффа. Как измерить осмотическое давление? Как вычислить осмотическое давление?
3. Какие растворы называют изотоническими? Что такое гемолиз и плазмолиз?
4. Приведите разные формулировки 1-го закона Рауля.
5. Каков физический смысл криоскопической и эбулиоскопической констант? Каково прикладное значение криоскопии и эбулиоскопии?
6. Почему в речной воде глаза «режет», а в морской нет?
7. Почему осмотическое давление у семян и растений засушливых зон выше, чем у болотных растений?
8. Почему растворы кислот, оснований, солей не подчиняются законам идеальных растворов? Что такое изотонический коэффициент?
9. Что называется электролитом? Чем отличаются сильные электролиты от слабых?
10. От чего зависит степень диссоциации слабого электролита? Как она связана с константой диссоциации?
3.2. Аналитические задания
1. Имеются растворы формальдегида и глюкозы с равными молярными концентрациями. В каком растворе осмотическое давление больше? Каково будет решение задачи, если вместо растворов с равными молярными концентрациями взять растворы с равными массовыми долями?
2. Имеются три раствора следующих концентраций: а) 10 г/л сахара С12Н22О11, б) 10 г/л глюкозы С6Н12О6 и в) 10 г/л глицерина С3Н5(ОН)3. Какой из растворов будет гипертоничен, а какой гипотоничен по отношению к раствору глюкозы?
3. Имеются 25%-ные водные растворы мочевины СО(NН2)2, глицерина С3Н5(ОН)3, фруктозы С6Н12О6. В какой последовательности будут замерзать, а в какой закипать растворы при постепенном понижении или повышении температуры?
4. Раствор бензойной кислоты в бензоле обнаруживает изотонический коэффициент меньше 1. На что это указывает? Что больше в этом растворе: концентрация частиц или молярная концентрация бензойной кислоты?
5. Одинаково ли осмотическое давление 1 М растворов глюкозы, уксусной кислоты и азотной кислоты?
6. В каком случае растворы различных неэлектролитов, содержащие в равных количествах одно и то же число граммов растворенного вещества, будут замерзать при одинаковой температуре?
7. Растворы нитрата бария и сульфата алюминия содержат одинаковое количество молей в 1 л воды. Какой из этих растворов будет обладать большим осмотическим давлением, если кажущиеся степени диссоциации той и другой соли одинаковы?
8. Имеются растворы хлорида алюминия, сульфата железа (3), хлорида бария с моляльной концентрацией 0,1 моль/кг воды. Кажущиеся степени диссоциации солей в этих растворах примерно одинаковы. В какой последовательности будут замерзать растворы при охлаждении?
4. Приложение
Таблица 4.1. Давление насыщенного водяного пара при различных температурах
|
Температура, ТоС |
Давление, Р, Па |
Температура, ТоС |
Давление, Р, Па |
Температура, ТоС |
Давление, Р, Па |
|
0 |
610,4 |
14 |
1598,5 |
28 |
3780,0 |
|
1 |
657,2 |
15 |
1705,2 |
29 |
4005,0 |
|
2 |
705,2 |
16 |
1817,2 |
30 |
4242,2 |
|
3 |
757,3 |
17 |
1937,1 |
32 |
4753,0 |
|
4 |
813,3 |
18 |
2065,1 |
34 |
5318,0 |
|
5 |
871,9 |
19 |
2197,1 |
36 |
5940,0 |
|
6 |
934,6 |
20 |
2338,4 |
38 |
6623,0 |
|
7 |
1001,2 |
21 |
2486,4 |
40 |
7374,0 |
|
8 |
1073,2 |
22 |
2643,7 |
50 |
12334,0 |
|
9 |
1147,8 |
23 |
2809,1 |
60 |
19920,0 |
|
10 |
1227,9 |
24 |
2983,7 |
70 |
31160,0 |
|
11 |
1311,9 |
25 |
3167,7 |
80 |
43360,0 |
|
12 |
1402,5 |
26 |
3361,0 |
90 |
70100,0 |
|
13 |
1497,2 |
27 |
3565,0 |
100 |
101325,0 |
Таблица 4.2. Криоскопическая Ккр. и эбулиоскопическая Кэб. константы растворителей, град×кг/моль
|
Растворитель |
Тзамерз. оС |
Ккр. |
Рстворитель |
Ткип..оС |
Кэб. |
|
Бензол |
5,5 |
5,1 |
Ацетон |
56 |
1,5 |
|
Вода |
0 |
1,86 |
Бензол |
80,2 |
2,57 |
|
Камфора |
174,8 |
39,7 |
Вода |
100,0 |
0,516 |
|
Нафталин |
80,1 |
6,9 |
Сероуглерод |
46,3 |
2,29 |
|
Уксусная кислота |
16,65 |
3,9 |
Этиловый эфир |
34,5 |
2,00 |
|
Фенол |
41 |
7,3 |
Этиловый спирт |
78,3 |
1,11 |
|
Циклогексан |
6,5 |
20,2 |
Хлороформ |
61,2 |
3,88 |
Контрольное задание по теме: «Законы Вант – Гоффа и Рауля для растворов неэлектролитов и электролитов»
|
№ |
Содержание задания |
Вариант задания |
||||
|
1 |
2 |
3 |
4 |
5 |
||
|
1 |
Вычислите активность соли в водном растворе, если известны: -моляльность cm, моль/кг; -средний коэффициент активности γ± |
KBr 0,1 0,79 |
MgCl2 0,04 0,80 |
Pd(NO3)2 0,01 0,69 |
LaCl3 0,018 0,57 |
CaSO4 0,05 0,78 |
|
2 |
Вычислите ионную силу раствора, если даны: -масса воды mo, г; -масса соли, m, г |
Ca(NO3)2 200 3,285 |
Li2SO4 300 1,255 |
ВaCl2 125 0,417 |
Na3PO4 250 0,550 |
Al2(SO4)3 150 0,480 |
|
3 |
Определите, чему равно осмотическое давление раствора, если известны: -масса растворенного вещества m, г; -объем раствора V, л; -температура раствора, оС |
Глюкоза С6Н12О6 9 100 0 |
Глицерин С3Н8О3 46 500 +27 |
Сахароза С12Н22О11 34,2 400 +17 |
Рибоза С5Н10О5 300 1000 -7 |
Этиленгликоль С2Н6О2 31 200 +7 |
|
4 |
Вычислите давление пара водного раствора неэлектролита, если заданы: -массовая доля растворенного вещества ω,%; -температура, оС |
Мочевина СО(NН2)2 3 30 |
Глюкоза С6Н12О6 4 40 |
Глицерин С3Н8О3 2 50 |
Сахароза С12Н22О11 1 25 |
Этанол С2Н5ОН 5 20 |
|
5 |
Определите молярную массу водного раствора неэлектролита, если заданы: -температура замерзания, оС; -масса растворенного вещества, г; -масса воды, г Ккр.(Н2О) = 1,86 |
-1,86 18 100 |
-0,93 171 1000 |
-7,44 9,2 50 |
-4,65 46 200 |
-9,3 64 400 |
|
6 |
Вычислите кажущуюся степень диссоциации водного раствора соли, если известны: -концентрация раствора, моль/л; -осмотическое давление, кПа; -температура, оС |
CaCl2 0,2 1247,1 27 |
NaBr 0,12 492,3 17 |
KCl 0,1 467,7 20 |
MgSO4 0,05 229,5 27 |
Ba(NO3)2 0,15 1115,2 25 |
Банк комбинированных задач
Раствор, содержащий 0,4359 моль/л тростникового сахара, при 18оС изотоничен с раствором хлорида натрия, концентрация которого 14,616 г/л. Определите кажущуюся степень диссоциации хлорида натрия в растворе.
Сколько граммов этилового спирта должен содержать 1 л раствора, чтобы его осмотическое давление было таким же, как молярного раствора азотной кислоты, кажущаяся степень диссоциации которой в этом растворе 80%?
Какова концентрация (масс. доли, %) физиологического раствора поваренной соли, применяемого для подкожного вливания, если этот раствор изотоничен с осмотическим давлением крови, равным 8,104 105Па при нормальной температуре человеческого тела 37оС? Кажущуюся степень диссоциации поваренной соли принять равной 1.
Сколько граммов глицерина должен содержать 1 л раствора, чтобы его осмотическое давление было таким же, как и раствора, содержащего в 1 л при той же температуре 4,5 г формальдегида (СН2О)?
Вычислить концентрацию водного раствора мочевины, если раствор при 27оС изотоничен с 0,5 М раствором СаС12. Кажущаяся степень диссоциации раствора хлорида кальция 65,4%.
Давление пара раствора, содержащего 13,38 г нитрата кальция в 200 г воды, 99560 Па при 100оС. Вычислить кажущуюся степень диссоциации соли в указанном растворе.
Определите атмосферное давление, если 0,1 н раствор хлорида бария кипит при 99,6 оС. Кажущаяся степень диссоциации соли в данном растворе 75%. Давление пара чистой воды при температуре 99,6 оС равно 99,930 Па.
Раствор, содержащий 17,1 г сульфата алюминия в 100 г воды, замерзает при -4,19оС. Определите кажущуюся степень диссоциации соли в растворе.
Некоторое количество тростникового сахара растворили в 1000 мл воды. Давление пара полученного раствора при 100оС составило 100200 Па. Вычислите температуру кипения и осмотическое давление указанного раствора при 100оС. Плотность раствора сахара принять равной 1.
Вычислите температуру замерзания раствора 7,308 г хлорида натрия в 250 г воды, если при 18оС осмотическое давление указанного раствора 2,1077 106 Па. Плотность раствора принять равной 1.