Известно, что СТ-ергическая система относится к стресс-лимитирующим системам (Меерсон, 1986), играет важную роль в регуляции болевой чувствительности. Вместе с тем имеющиеся в литературе данные свидетельствуют о том, что СТ обладает как обезболивающим (Yaksh, 1981; Advokat, 1993), так и проноцицептивным действием (Eide, Hole, 1993; Bardin et al., 2000). Многочисленные нейроны ядер центрального серого вещества, шва ствола и среднего мозга и широкая сеть аксонов, проецирующихся в различные структуры головного и спинного мозга, традиционно рассматриваются как одно из главных звеньев эндогенной обезболивающей системы. Так, например, в исследованиях R. D. Olesеn (1992) показано, что электрическая стимуляция у животных области дорсального шва и вентральной части центрального серого вещества вызывает подавление как функциональной, так и патологической боли, связанное с активацией СТ-ергической системы. Также выявлено, что увеличение порогов боли после иммобилизации (Brattacharya, 1978), термического стресса (Kulkarni, 1980), электрокожного раздражения (Shimuzu, 1981) снижается у животных, подвергнутых внутрибрюшинному введению DL-парахлорфениланалина (ПХФА) – ингибитора триптофангидроксилазы, и восстанавливается при введении СТ (Richter-Levin, Segal, 1989). Вместе с тем, в исследовании M. D. Tricklebank с соавт. (1984) доказано, что СТ-ергическая система выполняет тормозную функцию в процессах активации противоболевых систем при кратковременном болевом стрессе и активирующую – при других воздействиях. Однако участие данной системы в обеспечении антиноцицептивного эффекта низкоинтенсивного ЭМИ КВЧ не изучено.
В связи с вышеизложенным, задачей данной части исследования явилось изучение роли СТ в механизме антиноцицептивного действия низкоинтенсивного ЭМИ КВЧ при экспериментально вызванной тонической боли у крыс. Для решения поставленной задачи экспериментальных животных разделили на четыре равноценные группы по пять особей в каждой (рис 7.1).
Животных 1-ой группы подвергали только инъекции формалина (ФТ). У крыс 2-ой (ПХФА+ФТ) и 4-ой (ПХФА+КВЧ+ФТ) групп вызывали ингибирование синтеза СТ с помощью внутрибрюшинной инъекции растворенного в физиологическом растворе ПХФА («Sigma», США). Данный препарат вводили из расчета 300 мг/кг (Брагин, 1991, Marlene et al., 1999). Известно, что данный препарат вызывает изменение обмена СТ как в периферической нервной системе, так и в нейронах головного и спинного мозга (Fuller, 1995). Так, биохимическими исследованиями установлено, что ПХФА приводит к резкому уменьшению СТ у крыс по сравнению с контролем в среднем на 88 % в головном и на 78 % в спинном мозге (Брагин, 1991). Крысам 1-ой (ФТ) и второй (КВЧ+ФТ) групп внутрибрюшинно вводили эквивалентный объем физиологического раствора (0,9 % раствор NaCl). Эксперименты проводились через 72 часа после введения препаратов (Гура и др., 2002). Животных 3-ей (КВЧ+ФТ) и 4-ой (ПХФА+КВЧ+Ф) групп непосредственно перед инъекцией формалина подвергали воздействию ЭМИ КВЧ.
Как показали результаты исследования, при дополнительной внутрибрюшинной инъекции ПХФА – ингибитора синтеза СТ – у животных второй группы (ПХФА+ФТ) отмечалось увеличение общей продолжительности болевой реакции на 28,53 % (p<0,05) относительно значений у животных, подвергнутых только инъекции формалина. Длительность первой острой фазы «формалинового теста» имела тенденцию к уменьшению на 18,58 % (p>0,05), однако продолжительность второй тонической фазы увеличилась на 37,29 % (p<0,05) по сравнению с данными показателями у крыс первой группы (ФТ) (табл. 7.4; рис. 7.12, 7.13), что подтверждается и увеличением КМ при воздействии ПХФА до +0,3 усл. ед. (первая фаза – -0,19 усл. ед., вторая – +0,39 усл. ед.) (рис. 7.14). К концу 60-ти минутного наблюдения после инъекции формалина болевая реакция отмечалась на достаточно высоком уровне (32,00 ± 8,34).
Таблица 7.4.
Общая продолжительность поведенческих реакций (с) у крыс в «формалиновом тесте» (ФТ) на фоне предварительной инъекции парахлорфенилананина (ПХФА), воздействия электромагнитного излучения крайне высокой частоты (КВЧ) и их комбинированного действия (ПХФА+КВЧ) (![]() )
)
| Поведенческие реакции | Экспериментальные группы воздействия | |||
| ФТ(1) | ПХФА+ФТ(2) | КВЧ+ФТ(3) | ПХФА+КВЧ+ФТ(4) | |
| Общая болевая реакцияВ том числе: | 910,67±21,32 | 1181,00±31,11Р1,2<0,001
Р2,3<0,001 Р2,4<0,001 |
486,80±29,82Р1,3<0,001
Р2,3<0,001 Р3,4<0,001 |
888,50±34,15Р2,4<0,001
Р3,4<0,001 |
| Первая острая фаза | 144,00±7,70 | 117,25±6,92 р1,2<0,05Р2,3<0,001
Р2,4<0,05 |
33,20±9,02 р1,3<0,001Р2,3<0,001
Р3,4<0,01 |
84,25±11,35 р1,4<0,01Р2,4<0,05
Р3,4<0,01 |
| Вторая тоническая фаза | 766,67±25,40 | 1063,75±33,56 р1,2<0,001Р2,3<0,001
Р2,4<0,001 |
453,60±26,60 р1,3<0,001Р2,3<0,001
Р3,4<0,001 |
804,25±28,77 р2,4<0,001р3,4<0,001 |
| Бег | 136,83±10,07 | 76,25±10,87 р1,2<0,01р2,3<0,001
Р2,4<0,02 |
371,40±27,04 р1,3<0,001р2,3<0,001 р3,4<0,001 | 134,25±14,07р2,4<0,02
р3,4<0,001 |
| Груминг | 34,67±4,55 | 34,50±3,80 р2,3<0,01 | 200,60±31,99 р1,3<0,001р2,3<0,01
р3,4<0,01 |
46,25±14,45р3,4<0,01 |
| Прием пищи | 1,83±0,91 | 3,00±1,47р2,3<0,001
р2,4<0,01 |
28,40±4,20р1,3<0,001
р2,3<0,001 |
18,50±2,90р1,4<0,001
р2,4<0,01 |
| Сон | 0,00±0,00 | 0,00±0,00 | 0,00±0,00 | 0,00±0,00 |
| Покой | 2516,00±21,77 | 2305,25±41,02 р1,2<0,01р2,3<0,02
р2,4<0,05 |
2512,80±46,03Р2,3<0,02 | 2488,25±65,24р2,4<0,05 |
Примечание: р1-4 – достоверность отличий по критерию Стьюдента при сравнении с данными групп, обозначенными в таблице 1-4 соответственно.
У животных этой группы изменилась продолжительность и неболевых поведенческих реакций. Так, общая длительность двигательной активности уменьшилась на 34,38 % (p<0,05) (продолжительность реакции бега уменьшилась на 44,28 % (p<0,01), а приема пищи, наоборот, увеличилась на 63,64 % (p<0,01)). Продолжительности пассивного поведения и реакции груминга достоверно не изменились по сравнению со значениями соответствующих показателей у крыс первой группы (ФТ) (табл. 7.4; рис. 7.12, 7.15).
|
|
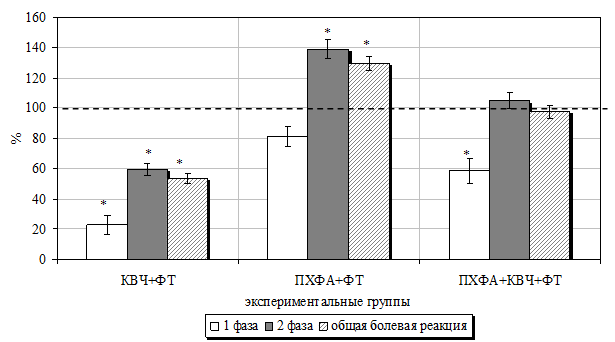
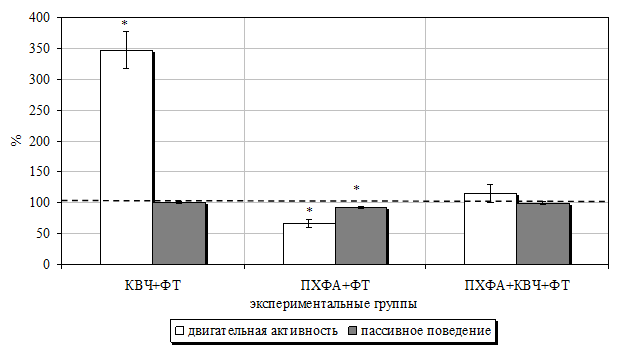
Рис. 7.12. Изменение продолжительности болевой (первой острой и второй тонической фаз) (А) и неболевых (двигательной активности и пассивного поведения) (Б) поведенческих реакций у крыс в «формалиновом тесте» (ФТ) на фоне предварительного воздействия электромагнитного излучения крайне высокой частоты (КВЧ), введения DL-парахлорфенилаланина (ПХФА) и их комбинации (в % относительно значений у животных, подвергнутых изолированному действию болевого фактора, принятого за 100 %).
Примечание *– достоверность различий по критерию Стьюдента относительно значений у животных, подвергнутых изолированному действию болевого фактора.
Эти данные свидетельствуют о том, что под влиянием ПХФА у животных в «формалиновом тесте» развивается общий двигательный дефицит и защитная реакция «затаивания». Следовательно, у крыс второй группы на фоне действия ПХФА произошло увеличение проявлений болевого стресса, что доказывает важную роль СТ-ергической системы в лимитировании развития стресс-реакции, в аналгетическом действии при болевых стрессах и согласуется с данными других исследователей (Kulkarni, 1980, Shimizu, 1981, Datla, 1996, Лиманский, 2003).
При предварительном воздействии ЭМИ КВЧ у животных третьей группы (КВЧ+ФТ) наблюдались достоверные изменения болевой и неболевых поведенческих реакций относительно значений соответствующих показателей у животных первой группы (ФТ) (табл. 7.4; рис. 7.12), что согласуется с данными первой серии экспериментов (раздел 4.1.1) и является подтверждением антиноцицептивного действия ЭМИ КВЧ при тонической боли.
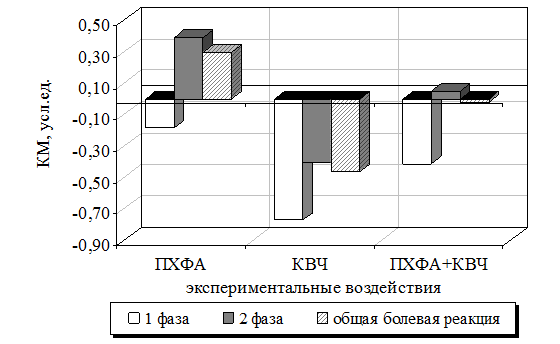
Рис. 7.13. Коэффициенты модифицирующего действия (КМ, усл. ед) экспериментальных воздействий (введения парахлорфенилаланина (ПХФА), воздействия электромагнитного излучения крайне высокой частоты (КВЧ) и их комбинированного действия (ПХФА+КВЧ)) на продолжительность болевой поведенческой (первой острой и второй тонической фаз) реакций при тонической боли у крыс.
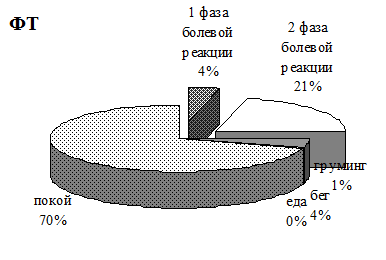
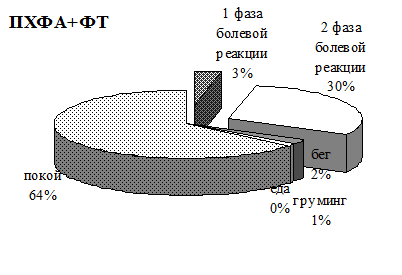


Рис. 7.14. Соотношение длительности поведенческих реакций (%) в течение 60-ти минут наблюдения у крыс в «формалиновом тесте» (ФТ) на фоне предварительной инъекции ингибитора синтеза серотонина парахлорфенилананина (ПХФА), воздействия электромагнитного излучения крайне высокой частоты (КВЧ) и их комбинированного действия (ПХФА).
При дополнительной инъекции ПХФА животным четвертой группы (Н+КВЧ+ПХФА), напротив, произошло увеличение продолжительности болевой реакции на 79,46 % (p<0,001) по сравнению со значениями этого показателя у крыс третьей группы, подвергнутых воздействию ЭМИ КВЧ и инъекции формалина без предварительного введения ПХФА. Так, длительность первой острой фазы «формалинового теста» увеличилась на 103,01 % (p<0,001), а второй тонической фазы – на 77,30 % (p<0,001) относительно значений данных показателей у животных третьей группы (КВЧ+ФТ) (рис. 7.4; рис. 7.12). Затухание болевой реакции у крыс данной четвертой группы к концу 60-тиминутного наблюдения не отмечалось (13,50 ± 1,94). Об уменьшении антиноцицептивного действия ЭМИ КВЧ под влиянием ПХФА свидетельствует и увеличение КМ от -0,47 (первая фаза – -0,74, вторая – -0,41) у крыс, которые подвергались КВЧ-воздействию без введения ПХФА до -0,02 (первая фаза – -0,41, вторая фаза – +0,05) у крыс четвертой группы (рис. 7.13).
Анализ длительности неболевых поведенческих реакций показал, что продолжительность двигательной активности уменьшилась на 67,77 % (p<0,01) относительно значений у животных третьей группы (КВЧ+ФТ). Длительность пассивного поведения у животных четвертой группы соответствовала таковой у крыс третьей группы, которым ПХФА не вводили (рис. 7.12, 7.14). При этом продолжительности изученных болевых и неболевых поведенческих реакций с большой степенью достоверности приближалась к значениям этих показателей в первой группе животных (ФТ) (рис. 7.12).
Следовательно, внутрибрюшинное введение ПХФА (300 мг/кг) привело к уменьшению антиноцицептивного действия ЭМИ КВЧ при экспериментально вызванной тонической боли (на 79,46 %; p<0,001), что указывает на участие СТ в механизме аналгетического действия ЭМИ КВЧ.
Автор — Джелдубаева Эльвиза Рашидовна