Исследования последних лет продемонстрировали важную роль системы эндогенных ОпП в развитии стресс-реакции организма, в регуляции уровня болевой чувствительности и модуляции эмоционального, поведенческого, вегетативного и других компонентов этих реакций (Amir et al., 1980; Лиманский, 1986, Holaday et al., 1983).
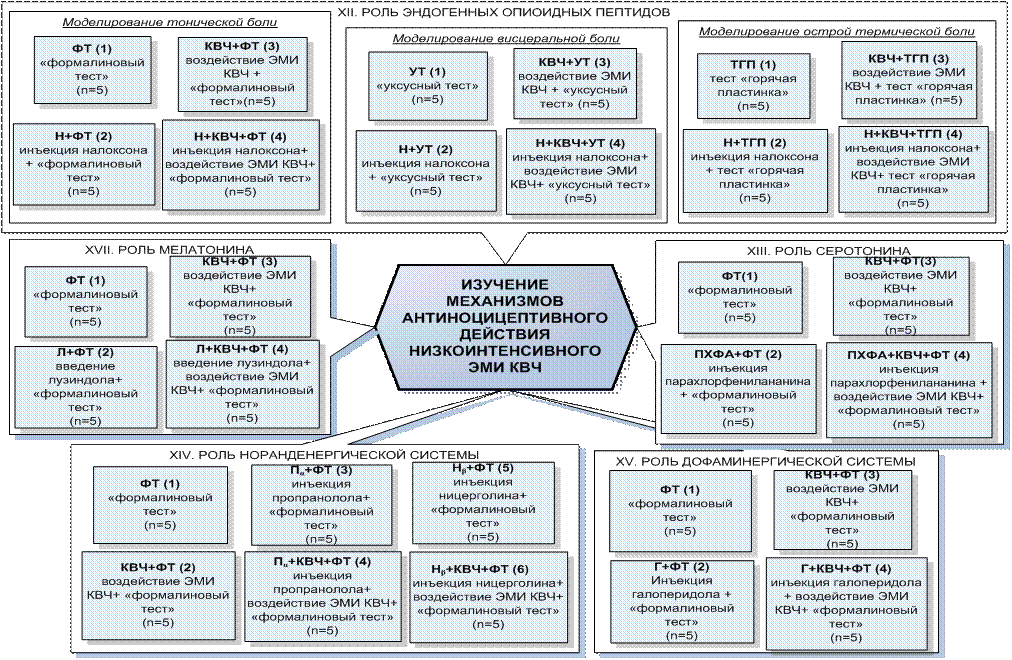
Рис. 7.1. Схема организации экспериментов по изучению механизмов аналгетического действия низкоинтенсивного электромагнитного излучения крайне высокой частоты (ЭМИ КВЧ), где ФТ – «формалиновый тест», ТГП – тест «горячая пластинка», УТ – «уксусный тест»; КВЧ – воздействие ЭМИ КВЧ; Н – внутрибрюшинная инъекция блокатора опиоидных рецепторов налоксона; ПХФА – внутрибрюшинная инъекция ингибитора синтеза серотонина DL-парахлорфенилананина; Г – внутрибрюшинная инъекция блокатора дофаминергических рецепторов галоперидола; Пα – внутрибрюшинная инъекция блокатора α-адренергических рецепторов пропраналола, Нβ – внутрибрюшинная инъекция блокатора β-адренергических рецепторов ницерголина; Л – внутрибрюшинная инъекция блокатора мелатониновых рецепторов – лузиндола.
Данные по изучению распределения ОпР, их лигандов в мозге, биохимических и фармакологических свойств ОпП, а также экспериментов, проведенных с применением одного из наиболее известного и широко применяемого антагониста ОпР – налоксона явились основой для предположения, что различные виды обезболивания обеспечиваются, главным образом, опиоидергической системой организма (Przewlocki, 2001; Stein, 1995, Fields, 1999). Вместе с тем, экспериментальные исследования с использованием налоксона имеют противоречивые данные о его способности угнетать эффекты различных видов обезболивания. Так, у крыс частичное увеличение болевой чувствительности в присутствии налоксона установлено при неизбегаемом болевом стрессе (Брагин, 1986), плавании в холодной воде (Buckett, 1979), в «формалиновом тесте» (Кулікович та ін., 1999), но в ряде других исследований влияния налоксона на уровень болевой чувствительности не отмечалось (Hayes, 1978, Rodgers, 1981). Различие конечных эффектов при действии налоксона, очевидно, обусловлено разнообразием нейрохимического и нейроморфологического обеспечения механизмов регуляции болевой чувствительности и связано с разной степенью активации опиоидных механизмов обезболивания, которая, в свою очередь, определяется условиями проведения эксперимента. Однако участие системы эндогенных ОпП в механизмах антиноцицептивного действия ЭМИ КВЧ (7,1 мм, 10мВ/см2) не исследовано. Вместе с тем на вовлеченность опиоидной системы в реализацию биологических эффектов, вызываемых микроволновым излучением, указывается многими исследователями (Kavaliers et al., 1994; Lai et al., 1998; Ковешников и др., 2000; Штемберг и др., 2000, Чуян, Махонина, 2005).
В связи с вышеизложенным задачей данной серии экспериментов явилось исследование системы эндогенных ОпП в механизме антиноцицептивного действия низкоинтенсивного ЭМИ КВЧ при болевом стрессе у крыс.
Для реализации поставленной задачи экспериментальных животных разделили на двенадцать равноценных групп по пять особей в каждой (рис. 7.1). В первой серии у крыс первой-четвертой групп болевой стресс моделировали в «формалиновом тесте» (ФТ) (тоническая боль). Животным второй (Н+ФТ) и четвертой (Н+КВЧ+ФТ) групп за 15 минут до экспериментальных воздействий (болевой стресс, воздействие ЭМИ КВЧ) внутрибрюшинно вводили растворенный в физиологическом растворе налоксон («Sigma», США). Данный препарат является ((-)-17-аллил-4,5(-эпокси-3,14-дигидроксиморфин-6-он) гидрохлорида дигидратом, принадлежит к группе неселективных блокаторов всех субтипов ОпР, устраняет центральное и периферическое действие опиоидов, включая эндогенные эндорфины, проникает через гематоэнцефалический и плацентарный барьеры. После парентерального введения налоксон быстро распределяется по организму, период его полувыведения во взрослом организме составляет от 30 до 81 минуты (в среднем 64±12 минуты) (Martin W, 1976). Налоксон вводился из расчета 10 мг на 1 кг веса животного. Данная доза препарата является достаточной для блокирования практически всех типов ОпР (Брагин, 1991, Dogrul, 2005). Крысам первой (ФТ) и третьей (КВЧ+ФТ) групп подкожно вводился эквивалентный объем физиологического раствора (0,9 % раствор NaCl).
Непосредственно перед ФТ животные третьей (КВЧ+ФТ) и четвертой (Н+КВЧ+ФТ) групп дополнительно подвергались превентивному воздействию ЭМИ КВЧ.
Во второй серии первую-четвертую группу составляли животные, у которых болевой стресс вызывали в «уксусном тесте» (УТ) (висцеральная боль). Животным второй (Н+УТ) и четвертой (Н+КВЧ+УТ) групп за 15 минут до экспериментальных воздействий вводили раствор налоксона (10 мг/кг), а крысам первой (УТ) и третьей (КВЧ+УТ) групп – эквивалентный объем физиологического раствора. Животные третьей (КВЧ+УТ) и четвертой (Н+КВЧ+УТ) групп подвергались предварительному 30-ти минутному КВЧ-воздействию.
Показателями интенсивности болевой реакции у крыс при экспериментально вызванной тонической боли служила продолжительность лизания пораженной конечности, а висцеральной боли – длительность тонических поз (корчи) и реакции вылизывания живота. Неболевые поведенческие реакции были рассмотрены в аспектах продолжительности двигательной активности (бег, груминг, прием пищи) и пассивного поведения (сон, покой).
В третьей серии животных 1 – 4-ой групп подвергали воздействию острой термической боль в тесте «горячей пластинки» (ТГП) с определением БП и УВБ. Животным второй (Н+ТГП) и четвертой (Н+КВЧ+ТГП) групп за 15 минут до экспериментальных воздействий внутрибрюшинно вводили налоксон (10 мг/кг), а крысам первой (ТГП) и третьей (КВЧ+ТГП) групп – эквивалентный объем физраствора. Непосредственно перед термическим воздействием животных третьей (КВЧ+ТГП) и четвертой (Н+КВЧ+ТГП) групп подвергали воздействию низкоинтенсивного ЭМИ КВЧ.
Автор — Джелдубаева Эльвиза Рашидовна