Цель занятий. Изучить этиологию, патогенез и проявления нарушений кислотно-основного равновесия у животных с патологией обмена веществ в эксперименте.
Задание 1. Изучить механизмы нарушений кислотно-основного равновесия. Изменение резервной щелочности крови собаки, у которой удалена поджелудочная железа.
Оснащение: сдвоенные колбы по И. П. Кондрахину, подготовленные к титрованию; микробюретка на 2 мл (15); 0,02 н. раствора серной кислоты (0,01 моль/л) (50 мл); 1%-ный раствор фенолфталеина (10 мл).
Постановка опыта. За день до занятия в хозяйстве или стационаре клиники получают кровь от больных животных и подготавливают ее к исследованию диффузионным методом с помощью сдвоенных колб по И. П. Кондрахину.
В чистую, сухую центрифужную пробирку помещают 1 мл вазелинового масла и 20 ЕД гепарина на 1 мл крови, 2-5 мл крови, взятой из яремной вены, вносят в подготовленную пробирку, закрывают ее пробкой и кровь осторожно перемешивают с антикоагулянтом. От каждого животного кровь берут в отдельную пробирку, на которой ставят номер. Пробирки доставляют в лабораторию, где их центрифугируют в течение 20 мин при 3000 об./мин и помещают в холодильник при температуре 4°С. По количеству проб крови с учетом параллельных исследований подготавливают сдвоенные колбы. Для контроля оставляют не менее трех сдвоенных колб. Все колбы закрывают резиновыми пробками и открывают только в момент внесения реактива, после чего сразу опять закрывают. Точность результатов всей серии исследований зависит от точности титрования гидроокиси натрия в контрольных колбах.
На левых колбах всех пар ставят номера, соответствующие номерам проб крови на пробирках, или букву «К» на контрольных колбах. В правые колбы всех пар из бюретки вливают по 2 мл 0,02 н. (0,02 моль/л) раствора натрия гидроксида, в смежные (левые) колбы (кроме контрольных) вносят пипетками (не выдувая) по 0,5 мл плазмы крови, находящейся под вазелиновым маслом. Во всех случаях, когда реактивы вводят в колбы пипетками, их не выдувают, а дают свободно стекать. Затем во все левые колбы из бюретки или пипеткой поочередно вносят по 1 мл 5%-ного раствора серной кислоты (0,5 ммоль) и быстро плотно закрывают колбы пробками. Вращательными движениями перемешивают плазму крови с кислотой (не менее трех раз). Колбы оставляют на ночь. На следующий день приступают к титрованию.
Каждый студент получает 3-4 сдвоенные колбы, подготовленные для титрования в предыдущий день. Титруют содержимое правых колб, а обозначения (К – контроль, № животного) пишут на левых колбах. Все колбы должны быть плотно закрыты, их открывают только в момент внесения реактивов.
Поочередно титруют содержимое колб. Для этого открывают правую колбу с раствором натрия гидроксида и вносят в нее 1-2 капли раствора фенолфталеина, затем из микробюретки на 2 мл, заполненной 0,01 моль/л (0,02 н.) раствором серной кислоты, титруют до полного обесцвечивания раствора. Скорость титрования контрольных и опытных проб должна быть одинаковой. Результаты титрования записывают в таблицу и рассчитывают резервную щелочность (X) В объемных процентах СОз на 100 мл плазмы крови по формуле
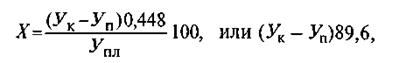
Где Ук – количество 0,01 моль/л раствора серной кислоты, пошедшее на титрование контроля, мл; Уп – количество 0,01 моль/л раствора серной кислоты, пошедшее на титрование исследуемого образца, мл; Упл – количество плазмы крови (в методике принято равным 0,5), мл; 0,448 – коэффициент данной реакции; 100 – коэффициент для пересчета результатов анализа на 100 мл плазмы крови.
Оформление протокола опыта. В протоколе кратко излагают постановку опыта и записывают показатели щелочного резерва крови у интактной и депанкреатизированной собак. Делают выводы. Объясняют механизм нарушения и компенсации кислотно-основного равновесия у собаки с удаленной поджелудочной железой.
В норме щелочной резерв у крупного рогатого скота — 46-66, у овец — 48—60 об.% СО2. Делают выводы. Объясняют механизм нарушения кислотно-основного равновесия. Называют вид нарушения.
Нормальные показатели щелочного резерва крови составляют: у собак 40-60 об.% СО2, у овец 50-52, у крупного рогатого скота 46-
54 об.%СО2.
Задание 2. Гипогликемическая кома у мыши.
В организме животных углеводы участвуют в разнообразных метаболических реакциях, взаимодействуя с белками и липидами. Одна из главных функций углеводов состоит в том, что они представляют собой основной энергетический субстрат для клеток всех тканей, но особенно нервной. Установлено, что 67 % глюкозы крови потребляют клетки центральной нервной системы.
Углеводы поступают в организм с растительной и животной пищей в виде моно-, ди — и полисахаридов. Может быть избыточное, а чаще недостаточное снабжение животных углеводами. Последнее обстоятельство сразу сказывается на межуточном обмене веществ, так как для энергетических целей начинают использоваться жиры и в какой-то степени белки.
Недостаточная обеспеченность организма углеводами возможна в результате нарушения процессов переваривания и всасывания. Например, при недостаточном поступлении гликолитических ферментов поджелудочной железы и кишечного сока (амилаза, лактаза). Полное расщепление углеводов до сахаров в тонком кишечнике не всегда завершается всасыванием. Уровень углеводов в крови поддерживается нейрогуморальными механизмами.
Уровень глюкозы в крови здоровых взрослых животных колеблется (мг/100 мл): крупный рогатый скот — 40-60, лошади — 55-95, свиньи — 45-75, собаки — 60-80, куры — 80-140, кролики — 75-85.
У больных животных эти показатели могут существенно меняться за счет интенсивности поступления углеводов, синтеза гликогена, уровня потребления глюкозы, соотношения этих процессов.
Под гипогликемией понимают уменьшение содержания глюкозы в крови. Основные ее причины:
Недостаточное поступление углеводов с кормами; снижение гидролиза сахаров в кишечнике и замедление их всасывания; повышение тонуса парасимпатической иннервации; недостаточная выработка глюкокортикоидов, соматотропного и адренокортикотропного гормонов передней доли гипофиза; повышение секреции инсулина, обусловленное гиперплазией островкового аппарата поджелудочной железы, развитием (у собак) раковой опухоли; развитие гепатопатий (гепатит, острая жировая дистрофия, цирроз) с подавлением гликогенообразовательной функции;
Гипофизарная кахексия; интенсивная мышечная работа, особенно у лошадей при длительных переходах, перевозке грузов; передозировка инсулина, вводимого животным с лечебной целью.
Последствия гипогликемии обусловлены, прежде всего, изменениями деятельности центральной нервной системы. Глюкоза для ее клеток является основным энергетическим субстратом. Недостаток сахара приводит к истощению энергетических резервов, усилению катаболических процессов, гипоксии структур мозга, внутриклеточной гипергидратации. Повышение проницаемости стенок сосудов сопровождается отеком мозга, возможностью кровоизлияний и тромбоза.
У жвачных животных возможно развитие гипогликемического синдрома, проявляющегося первоначально астеническим состоянием, затрудненностью передвижения. В последующем наблюдается беспокойство, появляются дрожь, клонические и тонические судороги, обильная саливация, непроизвольные дефекация и мочеиспускание. Одышка, тахикардия, зрачки расширены. Возможно развитие коматозного состояния.
Оснащение: шприцы на 1 мл с иглами; инсулин (1 флакон); 10%-ный раствор глюкозы (10 мл); подопытные животные: мыши.
Постановка опыта. Гипогликемическую кому воспроизводят с помощью инсулина. Мышей перед опытом выдерживают сутки без корма. Дачу воды не ограничивают.
Подопытным мышам вводят инсулин под кожу по 0,25 ЕД на животное. Другой группе мышей одновременно с инсулином в брюшную полость вводят по 1 мл 10%-ного раствора (0,55 моль/л) глюкозы. Наблюдают за поведением животного.
Оформление протокола опыта. Кратко записывают условия опыта и подробно излагают изменения в поведении мышей. Сравнивают поведение мышей, которым вводили только инсулин, с поведением животных, которым кроме инсулина инъецировали также глюкозу. Делают выводы. Объясняют профилактическое действие глюкозы.